El laboratorio de microbiología frente al bioterrorismo (página 2)
La respuesta mundial a los crecientes
peligros de las armas
biológicas, no ha satisfecho la esperanza requerida. El
tratado de 1972 para la no proliferación de armas
químicas y
biológicas, fue un paso útil
que cimentó el consenso internacional de que éste
tipo de armas era moralmente horrible. Las violaciones flagrantes
al pacto por las naciones que se habían comprometido a
cumplirlo, subraya sus inherentes debilidades.
Durante la "guerra
fría" a pesar de que predominó el concepto de lo
que se ha denominado como "ceguera nuclear", visión
definida como la actitud de que
el poder de
destrucción nuclear es tal que nada más puede
ser tomado en cuenta, Estados Unidos
continuó con un programa de armas
biológicas, al igual que Rusia,
desarrollándose dos sitios principales de producción de agentes biológicos:
Fort Detrick en Estados Unidos.
Al Hakam en Irak y
BioPreparat , Obolensk, Stepnogorsk, Vector, Sverdlovsk y la Isla
Vozrozhhdeniye en la Unión Soviética.
La batalla de gobierno
americano contra las cartas cargadas
de esporas ilustró las enormes lagunas científicas
respecto al Ántrax, uno de los gérmenes más
antiguos y más eficaces que los científicos
militares habían convertido en arma.
El 21 de Enero de 1999 el expresidente
norteamericano Bill Clinton manifestó en una conferencia de
prensa : " Ni
siquiera las armas nucleares o las armas químicas son tan
aterradoras como la guerra
bacteriológica. Aunque un ataque químico
sería finito, un ataque biológico se
extendería por la tierra,
sobre todo si los perpetradores liberaran un agente contagioso
que no fuera identificado rápidamente, ni tratado de
manera adecuada. Un ataque con gérmenes, sería un
regalo que va de mano en mano ".
Las toxinas biológicas son cientos e
incluso miles de veces más letales por unidad de peso que
cualquier agente químico conocido. Desde la perspectiva
militar, las armas biológicas tienen
diferentes tiempos para hacer su efecto, lo que las hace
impredecibles, y por lo tanto ejemplares para operaciones
clandestinas y/o guerra de baja intensidad.
Se estima que un arsenal biológico
puede ser producido en un espacio de no más de cinco
metros cuadrados y con una inversión de $ 10,000.00 en equipo. Por
esto, " la bomba atómica de los países pobres "
puede ser desarrollada por cualquier país a un costo muy bajo.
Se estima que el costo por atacar con armas convencionales a
civiles desprotegidos es de aproximadamente $ 2000.00 por
kilómetro cuadrado, de 800 dólares con armas
nucleares, 600 dólares con gases
químicos, y un dólar con el uso de armas
biológicas. ( Ref. Robinson p. The problems of
chemical and biological Warfare.1998. CB Weapons today.
).
Muestras de la biotecnología aplicada al terrorismo,
especialmente en el campo de la ingeniería
genética fueron los trabajos del equipo militar Ruso
de investigaciones
en los Institutos Obolensk y BioPreparat que manifestaban haber
podido reestructurar la legionella modificada con genes de
mielina, tal que aunque el microorganismo
fuera eliminado, aún permanecía en el
paciente síntomas de parálisis y daño
cerebral como reacción posterior por la infección
de esta cepa de Legionella recombinante. Igualmente se
trabajó en introducir en la bacteria de la peste (
Yersinia pestis ), el gen que crea la toxina de la difteria.
Así también cepas de Ántrax resistente a
antibióticos y a las vacunas, como
también cepas mortales con marcadores
étnicos.
La comunidad
internacional ha empezado a debatir si los ingenieros
genético y los médicos militares, deberían
adoptar su propia versión del juramento Hipocrático
: No hacer daño
Todo lo anterior nos permite hacer
válido en nuestros tiempos las palabras del estadista
americano Thomas Jefferson : El precio de la
libertad, es
la eterna vigilancia.
OBJETIVOS DE LAS ARMAS
BIOLÓGICAS
Los objetivos de
las armas biológicas dependen de lo que se pretende
conseguir, tanto en la población como en el ambiente; sin
embargo, ellas están dirigidas principalmente a
:
Seres humanos ( Combatientes o civiles
).Cosechas alimenticias.
Animales.
Plantas de tratamiento de
agua.Suelo.
Aire.
Combinaciones de varios
objetivos.
La utilidad de las
armas biológicas están dirigidas principalmente
para :
Eliminar a la población para
ocupar territorioEliminar o invalidar fuerzas militares
o estratégicasProducir terror
Objetivos políticos
El bioterrorismo en
la historia
El empleo de
agentes biológicos como arma no es un concepto nuevo. La
historia de su
uso ofrece numerosos ejemplos de su utilización aun antes
del desarrollo de
la microbiología. Existen evidencias que
sugieren que civilizaciones como las de los persas y romanos
contaminaban el agua potable
de pozos y acueductos de sus enemigos arrojando en ellos animales
muertos.
En el siglo VI AC Asirios envenenan los
pozos enemigos con desechos pútridos.
Durante el siglo XIV en el sitio de Kaffa
(ahora Feodossia ) en Ucrania, las fuerzas tártaras
sitiaron la ciudad y obligaron a rendirse a sus habitantes
infectándolos intencionalmente con Yersinia
pestis al lanzar con catapultas por sobre las murallas de la
ciudad los cuerpos sin vida de sus propios soldados muertos por
plaga. Esta enfermedad epidémica causó el
aniquilamiento de un tercio de la población europea de la
época. Esta misma estrategia
bélica fue utilizada por el ejército ruso contra
Suecia en 1710.
En 1532 en la conquista de
Perú, Francisco Pizarro reparte ropa ( frazadas ) de
muertos por viruela entre los Incas,
consiguiendo la diseminación de la viruela en forma muy
efectiva. Igual en EEUU, en 1763, Sir Jeffrey Amherst, comandante
de tropas británicas durante la guerra de independencia
de Estados Unidos, diseminó la viruela entre
los nativos americanos utilizando pañuelos y cobijas de
personas que habían muerto de viruela.
Entre 1937 y 1941 en la unidad 731, se
experimentó en Ping Fang Manchuria una amplia gama de
agentes virales y bacterianos, especialmente Antrax,
inoculándolos directamente o a través de aire, agua o
alimentos
contaminados tanto en animales como en humanos, causando la muerte de
más de 10,000 personas. Con posterioridad a la Segunda Guerra
Mundial se estimó que alrededor de 3000 prisioneros
murieron en relación a estos experimentos. En
1940, se produjo una epidemia de plaga en China y
Manchuria, su inicio se relacionaron con una "lluvia de pulgas"
infectadas con Yersinia pestis arrojadas por aviones
japoneses que sobrevolaron la zona afectada.
En 1979 una falla en los sistemas de
filtración dio origen a un pequeño aerosol
de esporas de ántrax, que se diseminó en la
población de Sverldovsk, originando 79 casos de
ántrax de los que 66 murieron. En 1984 Durante un solo mes
en Dallas, Oregon, 751 personas desarrollaron
gastroenteritis por Salmonella luego de la
contaminación de los "salad bar" en varios
restaurantes por el culto religioso Rajneeshees.
En el año 2001 los casos de contaminación por Anthrax en EEUU fueron
actos terroristas.
Característica
del arma biológica ideal
Las armas biológicas se caracterizan
por tener grandes ventajas como :
Cobertura de grandes
áreas.No producen daños al material
inerte.Son baratos al comparar con otras
armas.Difícil detección e
Identificación debido a los largos períodos
de incubación.
No detectable por nuestros sentidos :
Incolor, inodor.Permiten el progreso
Epidémico.
Por lo anterior, las características
de un arma biológica perfecta deben ser :
Alta infectividad ( Dosis infectante
baja ). Que requiera pocos organismos o
pequeña cantidad de material.
Que sea muy contagioso ( Rapida
diseminación ).Altamente letal.
De fácil diseminación y
estable en almacenamiento ( Listo para usar )Resistente a las condiciones
ambientales.Resistente a tratamiento ( Vacunas,
antibióticos, drogas, antídotos, etc
).
Creemos que ésta denominación
recae sin lugar a dudas en el
Ántrax.
Elementos que
sugieren un ataque bioterrorista
Durante la rutina diaria de los
microbiólogos, se tiene una idea razonable de los
microorganismos que están involucrados en los diferentes
procesos
infecciosos, por lo que la
investigación se enfoca en primer lugar en los agentes
típicos de los enfermedades infecciosas.
Sin embargo, cuando se trata de un ataque terrorista con armas
biológicas, el microbiólogo debe pensar primero en
lo menos probable, ya que los agentes involucrados no forman
parte de la rutina investigativa en los laboratorios de
microbiología. Por esto decimos que en caso de sospecha de
ataque bioterrorista, " Cuando oigas pasos sonar …
piensa primero en  ,
,
no en caballo "
Algunos elementos que pueden sugerir un
ataque bioterrorista pueden ser:
Epidemia sorpresiva de síndromes
clínicos específicos en población
definida.Aumento rápido de número
de enfermos procedentes de población sin factores de
riesgo.Muertes inexplicadas.
Brote de enfermedad más grave
que lo conocido.Muchos casos de enfermedad adquirida
por vía menos frecuente.Casos únicos de enfermedad
previamente inexistente.Brotes por cepas inusuales.
Brotes en humanos con casos en
animales.Mayor número de casos con
evolución fatal de los esperados.Brotes anunciados por grupos
terroristas.Inusual brote de enfermedad fuera de
temporada o área geográfica.Enfermedad inexplicada en adultos
jóvenes.Aumento de casos de parálisis
flácida aguda o erupciones en extremidades.Enfermo con una enfermedad inusual y
que está descrita como potencial arma biológica
en personas que no estaban expuestos a éstos agentes
por su trabajo, viajes, etc.
Ref. CDC- MMWR. October
19,2001/50(41);893-89
Por lo anterior, es importante tener
siempre presente que :
A diferencia de las sustancias
químicas, los efectos de los agentes biológicos
serán vistos en muchos casos en días
después de la exposición.El reconocimiento precoz de los casos (
la mayoría tiene signos inespecíficos ),
es vital para organizar un sistema de vigilancia que
evite la propagación masiva.

Defensas contra las armas
biológicas
UMáscara respiratoriaU : Los
filtros, normalmente de carbón activado, han de
bloquear las partículas mayores de un
micrometro.URefugioU : Lo mejor es un
habitación cerrada, aislada con un recubrimiento
plástico o de cualquier otro material aislante y
ventilación con aire filtrado.UDescontaminación.
UVacunación U: Para agentes
específicos. Para muchos agentes no se conoce
vacuna.UAntibióticosU : Son eficaces
frente algunas bacterias, pero no frente a todas.
( Ineficaces contra los virus.)
USistemas de detecciónU : La
mejor arma es la prevención.
Agentes
etiológicos de las armas biológicas
Desde el punto de vista práctico,
casi cualquier germen capaz de causar enfermedad, puede ser
utilizado como arma biológica, ya que cada uno tiene
características morfológicas, patológicas y
epidemiológicas que pueden ser aplicadas dependiendo del
daño que se quiera infligir. Sin embargo, en Centro para
el Control de
Enfermedades Transmisibles de Atlanta ( CDC ) ha hecho una
clasificación que es utilizada mundialmente. En dicha
lista se incluye tres categorías en función de
la facilidad de su transmisión y mortalidad
producida.
CATEGORIA A :
Requieren alta prioridad de
respuestaSe diseminan fácilmente o se
transmiten persona a personaProducen alta mortalidad, con potencial
para un gran impacto en salud pública.Pueden causar pánico y
desequilibrio socialRequieren acción
especial/intervención sanitaria
públicaEs necesario preparación previa
del personal
Entre ellos están :
Bacillus anthracis
(ántrax)Toxina del Costridium botulinum
(botulismo)Yersinia pestis (peste)
Variola mayor (viruela)
Francisella tularensis
(tularemia)Fiebre hemorragica viral ( Ebola,
Lassa, Marburg )
CATEGORIA B :
Se diseminan con facilidad
moderadaCausan morbilidad moderada y mortalidad
bajaRequieren refuerzos específicos
de la capacidad diagnóstica y aumento en la vigilancia
de la enfermedad
Incluye a
E. coli 0157:H7
Brucelosis
Shigella dysenteriae
Enterotoxina B de Estafilococcus
aureusVibrio cholerae
Burkholderia mallei
Burkholderia pseudomallei
Toxina del Cl. perfringes
CATEGORIA C :
Son fácilmente
disponibles.Presentan facilidad en su
producción y diseminación.Posee potencial para provocar alta
morbilidad y mortalidad, además de tener impacto
público importante.
Entre ellos
Hanta virus
Fiebre amarilla
TBC multirresistente
Cryptosporidium sp
Virus Nipah
Bioseguridad en el
manejo de agentes biológicos peligrosos
Las Normas de
trabajo en
microbiología obligan al establecimiento rutinario de
medidas estrictas en el manejo de especimenes potencialmente
peligrosos. Estas indicaciones se multiplican cuando se trata de
microorganismos potencialmente utilizables como armas
biológicas, debido a la letalidad reconocida de
éstos agentes. Por lo anterior recomendamos firmemente las
Normas del CDC de Atlanta al respecto. ( Ref. Primary
Containment For Biohazards: Selection, Installation and Use of
Biological Safety Cabinets. CDC/NIH. U.S. Department of
Health and Human Services. Public Health Service. Washington,
1995 ). (Biosafety in Microbiological and Biomedical
Laboratories. CDC/NIH. U.S. Department of Health and Human
Services, Public Health Service (4ª ed.). Washington, 1999
).

URiesgo en el laboratorio de
los agentes de bioterrorismoU :

PRECAUCIONES
Utilizar cabina de seguridad
biológica de nivel II ( BSL-2) ó III (
BSL-3).Evitar cualquier actividad en el
área del personal con riesgo de exposición y
especialmente la producción de aerosoles.Descontaminar el laboratorio
después de cada uso y descarte todo el material en
receptáculos apropiados. Esterilice la
bata.Evite tocarse las mucosas con las manos
( con o sin guantes ).
Las peores
amenazas
Las peores amenazas están como es de
esperar, dentro del grupo A , y
entre ellas describiremos a las principales :
Bacillus anthracis
Yersinia pestis
Francisella tularensis
Viruela
Toxina del Clostridium
botulinumFiebre hemorragica viral ( Virus de
Ebola, Lassa y Marburg ).
Todos estos microorganismos utilizan uno o
varias rutas de entrada al organismo, :
Ingestión (Gastrointestinal )
por contaminación del agua y alimentosInyección (Piel / Membranas
mucosas) por cortaduras, lesiones leves, etcInhalación (Respiratorio ).
Especialmente aerosol. Contaminación del
aire
a) Bacillus anthracis

UB. anthracis en agar
sangre
B. anthracis , un bacilo grampositivo
esporulado, fué la primera bacteria que se
identificó como causante de una enfermedad. Su nombre
deriva del griego Anthrakis que significa carbón, en
alusión al color negro de su
pústula, por lo que se le conoce también como
Carbunco. Ya El Génesis lo cita como causante de la V
Plaga de Egipto. Es una
enfermedad zoonótica caracterizada por la habilidad del
bacilo para formar esporas. El Carbunco natural es primariamente
una enfermedad zoonótica de herbívoros : Cabras,
ovejas, vacas, caballos y otros animales transmiten el bacilo por
medio de la piel, cuero, lana,
pelo, huesos, heces,
orina y saliva.
Es endémica en muchos países
como México,
Nicaragua, Argentina, Bolivia,
Perú, Africa central y
China. Las humanidad tuvo la suerte que dos de los más
grandes microbiólogos lo estudiaran : Roberto Koch
reprodujo la enfermedad en animales y Luis Pasteur creó la
primera vacuna ( animales ).
Los factores de virulencia que se conocen
son tres proteínas
denominadas en conjunto toxina del carbunco y un
polipéptido capsular antifagocitario.
Ellos son el Factor Edema (FE), el Factor
Letal (FL) y el Factor Antígeno protector (AP). Los genes
encargados de elaborar la toxina del carbunco y el
polipéptido capsular se hallan en plásmidos de B.
Anthracis independientes. La combinación de los factores
en una cepa produce los signos
clínicos específicos, así :
FE + AP : Produce edema.
AP + FL : Producen la actividad
letal.
FE + FL : Inactivo.
AP + FL + FE : Produce edema y necrosis y
es letal.
La toxina del Factor Letal (LF) del Anthrax
afecta las células
dendríticas y disminuye la respuesta inmune para combatir
el microorganismo ( Ref. Nature. Emory University. July 17,
2003 ).
Algunas características
clínicas son :
Dosis infectiva (LD50): 8,000 – 15,000
esporasPeriodo de Incubación : 1-6
díasDuración de la enfermedad : 3-5
díasFiebre, malestar y fatiga
Abrupto distrés
respiratorio…muerte < 24 hrsNo hay transmisión de persona a
personaLos aislamientos son sensibles a las
drogas de elección : Doxyciclina y
Ciprofloxacina.
El ántrax es considerada el arma
biológica perfecta por sus características
:
Letal ( forma respiratoria )
Requiere dosis baja
Bajos costos de
producciónFácil almacenamiento
No detectable por los sentidos (
Inolor, Indolor )Resiste malas condiciones ambientales (
espora )Fácil de diseminar
Resistente a desinfectantes
La Oficina de
Evaluación de Tecnología del
Congreso Americano informó que un pequeño aeroplano
cargando 100 kg de esporas de ántrax podría
utilizar un fumigador para diseminar una dosis fatal para
3.000.000 de personas. Un informe de
la
Organización Mundial de la Salud estimó que si
un aeroplano libera 50 kg de ántrax a lo largo de 2 km en
la dirección del viento, sobre una
población de 500.000 personas, 95.000 podrían morir
y 125.000 serían incapacitadas.
Tiene tres formas de infección :
Inhalación, cutánea e intestinal.
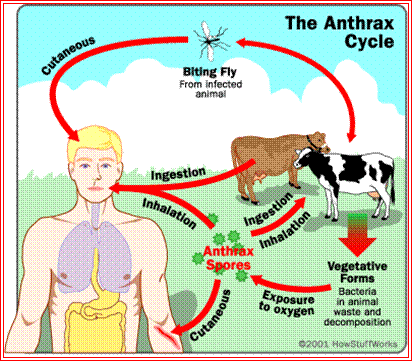
Ciclo del Anthrax
a1 ) Ántrax cutáneo
:
Ocurre al entrar en contacto la bacteria (
Espora ) con piel no intacta. Tiene un periodo de
incubación de 1 a 10 días. Produce una
pápula indolora, luego evoluciona a úlcera
necrótica típica. Esta es la forma más
común en casos naturales. Generalmente ocurre en la
cabeza, antebrazos y manos, causando inicialmente un prurito,
luego evoluciona a una pápula y luego a una escara negra
hundida, rodeada de edema.

a2) Ántrax intestinal
:
La forma intestinal de Antrax puede seguir
al consumo de
alimentos, especialmente carne de animales contaminados,
caracterizado por una inflamación intestinal aguda. Perido de
incubación de 1 a 10 días.
Los signos iniciales son náusea,
pérdida de apetito, vómito y
fiebre ,
seguido de dolor abdominal, vómito y severa diarrea
sanguinolenta.
Tiene una mortalidad entre el 50% – 100%,
especialmente en niños.
c3 ) Ántrax por inhalación
:
Las esporas de ántrax aerosolizado
causan la forma respiratoria de la enfermedad (conocida
tradicionalmente como la enfermedad de los cargadores de
lana). Las Esporas son inhaladas y luego ingeridas por los
macrófagos . Pasan a alveolos y bronquiolos donde germinan
y producen toxinas que causan edema , hemorragia y efusión
pleural.
Luego de un período de
incubación de 1 a 5 días, el paciente desarrolla
una enfermedad prodrómica caracterizada por fiebre,
malestar, tos no productiva y malestar respiratorio. Un
período asintomático de 2 a 3 días puede
ocurrir, o el paciente puede progresar directamente a una
enfermedad fulminante con disnea severa, estridor, cianosis,
distrés respiratorio, mediastinitis hemorrágica,
shock séptico, meningitis (50%) y muerte. Una
vez que los síntomas ocurren, el ántrax inhalatorio
es usualmente fatal a pesar del tratamiento antibiótico (
Ciprofloxacina ).
Las cartas contaminadas con ánthrax
enviadas a los senadores Brokaw y Daschle y a algunos medios
periodísticos posterior al ataque a las Torres Gemelas de
New York, provocaron el caos mas grande en los sistemas de correo
del mundo. La aparición del primer caso de ántrax
pulmonar en Florida confirmó estas aprehensiones. Entre
octubre y noviembre del 2001 ocurrieron 10 casos de ántrax
pulmonar producto de
inhalación de esporas enviadas por correo en cartas o
paquetes. Mas de 125,000 muestras clínicas evaluadas. Un
millón de muestras ambientales estudiadas. Incluso fue
necesario la preparación de Manuales para la
vigilancia de las cartas en el correo. ( Ref. CDC –
Recommendation for Protecting Workers from Exposure to
Bacillus anthracis in Work Sites where Mail is Handled or
Processed. Oct 31, 2001 ). Todo lo anterior obliga a los
laboratorios a establecer protocolos de
trabajo para manejar casos similares en el futuro.
DIAGNOSTICO ETIOLOGICO DEL
ANTHRAX:
a) Especimenes aceptables:
1. Anthrax
cutáneo:
a. Etapa vesicular: Coleccione el
líquido vesicular de manera aséptica con un hisopo
estéril, de una vesícula no abierta.
Nota: Los bacilos del ántrax son
vistos con más probabilidad
por tinción de Gram en la etapa vesicular.
b. Etapa de Escara : Recoger el material de
la escara cuidadosamente
levantando el borde externo de la escara;
insertar un hisopo estéril, después
rotar lentamente debajo del borde sin
desprenderla.
2. Ántrax
gastrointestinal:
a. Cultivo de sangre: Recoger
el volumen de la
sangre y el número apropiados de botellas
según el protocolo del
laboratorio. En fases posteriores enfermedad (2-8
días post-exposición) los cultivos pueden
producir crecimiento del microorganismo,
especialmente si se obtienen antes del tratamiento
con antibióticos.
b. Heces: Transfiera = 5 g de las heces
directamente en un envase hermético, limpio,
seco, estéril y de boca ancha.
c. Hisopo Rectal : Para pacientes a los que
no se les puede recoger espécimen, obtenga
una muestra
insertando un hisopo rectal dentro del esfínter
anal.
3. Ántrax por
Inhalación:
a. Cultivo de sangre: Recoger el volumen de
sangre y el número apropiados de set
según el protocolo del laboratorio.
b. Esputo: Recoger > 1 ml de
espécimen del tracto respiratorio inferior en un
envase estéril. El ántrax de
Inhalación por lo general no da lugar a la
formación de esputo.
b) Transporte del
espécimen y almacenamiento:
1. Hisopos : Transportar directamente al
laboratorio a temperature ambiente. Para transporte
por > de 1 hora, transportar a 2 – 8°C.
2. Heces : Transportar las heces no
preservadas al laboratorio dentro de 1 hora. Para
transporter por > 1 hora, trasnporte a 2-8°C en medio de
Cary-Blair o equivalente.
3. Esputo : Transportar en envase
estéril, con tapa de rosca, a temperature ambiente.
Cuando el tiempo de
transporte es de > 1 hora, transporte a 2 –
8°C.
4. Hemocultivos : Transporte directamente
al laboratorio a temperature ambiente.
c) Cultivo :
c1) En la cabina de bioseguridad clase II o
III, inocule la muestra en medios de agar sangre al
5%, agar alcohol-fenil-etílico y Tioglicolato o su
equivalente.
c2) Incubar por 24 horas a 35 – 37 ?
C a temperatura
ambiente ( CO2 es aceptable ).
d) Lectura
:
Observe el crecimiento y haga las pruebas
bioquímicas necesarias para la identificación y
diferenciación del germen.
d1 ) Criterios de identificación
presuntiva :
Bacilos Grampositivos
Crecimiento característico en
agar sangre ( Colonias rugosas, de 2 a 5 mm de
diámetro, convexa, de bordes irregulares )Formador de esporas
Movilidad negativa
Catalasa positiva
Formación de cápsula (La
tinta china permite visualizar la cápsula en muestras
de sangre y LCR ).No hemolítica en agar
sangre
Criterio de descarte : La morfología
al Gram, la hemólisis o la movilidad, pueden descartar la
presencia del B. anthracis.


Frotis por Gram de B.
anthracis
Tips:
La especie más común de
Bacillus sp. enviado al CDC para descartar B.
anthracis es la variedad no motil de B.
megaterium.Diferenciar las colonias del B.
cereus var. mycoides.Inactivación en el laboratorio :
121º C por 45 minutos.
Ref. J. of Clin. Microb. Vol.41, No.2,
February 2003
UDIFERENCIACIÓN ENTRE BACILLUS
ANTHRACIS Y BACILLUS sp

Ref : Bioterrorism: Implications for
the clinical microbiologist. Clin. Microb. Review, April 2001,
p.364-381, Vol.14, No.2
Vacuna contra el Anthrax
:
La primera vacuna por Luis Pasteur
(1881).6 dosis (ya hay protección
después de 3era).Efectividad 93% para infección
cutánea y muy alta para respiratoria.Vacuna para animales no sirve para
humanos.Indicación limitada a personal
de laboratorios de ántrax, militares, trabajadores con
animales.La vacuna consiste en un filtrado
estéril no infeccioso de un cultivo de una cepa
atenuada de B. anthracis, absorbida a un adyuvante(
hidróxido de aluminio). BioThrax"¢ [BioPort
Corporation, Lansing, Michigan].El componente protectivo de la vacuna
es un extracto de antígeno protector.
Formaldehído (concentración final, 0,02% ) es
adicionada como estabilizador y cloruro de benzeno (0.0025 %
), como un preservativo.Es imposible contraer la enfermedad a
partir de la vacuna.
UDesinfección /
Destrucción de esporas de B.
anthracisU:
 Desinfectantes usados para destruir
Desinfectantes usados para destruir
las esporas del B. anthracis
Formalina al 2 a 10% por 30 minutos a
40 °CFormalina al 0.25% por 6 horas a
60°CAcido paracetico al 3% a razón
de 8 litros (2 galones) /metro cuadrado por 10
minutos.Hipoclorito del sodio (10.000 PPM) 5
–10 minutos a temperatura ambienteIodo a 100 –300 PPM por 1
–5 minutos a temperatura ambiente
 Uso del calor para
Uso del calor para
destruir el B. anthracis
Para pequeños volúmenes o
contaminación ligera, autoclavar a 121 Po PC por 30
minutos. Para bolsas de autoclave, etc. que contiene los materiales
usados y contaminados del laboratorio, platos de cultivo, etc,
autoclavar a 121°C por 60 minutos
 Fumigación:
Fumigación:
El formaldehído es un gas y es generado
hirviendo las soluciones del
gas en agua
( formalina ) o calentando
formaldehído fuertemente. El agua se
satura hasta aproximadamente 37%, por lo que la formalina
concentrado es 37% formaldehído.
( Ref. CDC- Manual of
Laboratory Diagnosis of Anthrax. Annex 5- T Disinfection and
Sterilization Practices). T
b) YERSINIA PESTIS :
A lo largo de la historia, Yersinia pestis,
agente causante de la Plaga o Peste Negra, una enfermedad
zoonótica que ha provocado más de 200 millones de
muertes, especialmente en el medioevo ( 1300´s ), luego del
contagio, una vez que llega al flujo sanguíneo del
enfermo, infecta sus ganglios linfáticos, formando los
'bubones'. Después, el patógeno llega a los
pulmones y la enfermedad se vuelve mortal. Constituye una
enfermedad de la antigüedad, de la que existen numerosas
narraciones bíblicas y medievales, y que ha permanecido
hasta nuestros días.
La transmisión al hombre es
mayor durante primavera y verano, época en la que se
incrementa la vida al aire libre y el contacto con los animales
responsables de la transmisión. Los roedores urbanos y
selváticos ( ratas, ardillas y coyotes ) y las pulgas son
los principales agentes transmisores de la enfermedad. El hombre se
contagia cuando es picado por las pulgas de las ratas infectadas.
La peste bubónica posee un período de
incubación de hasta una semana, tras la cual los
microorganismos proliferan en los ganglios linfáticos de
la región del cuerpo donde se produjo la
picadura.
Existen distintas formas clínicas,
de las cuales la más común es la forma
bubónica. Otras menos comunes, pero más graves son
la neumónica ( respiratoria ) , septicémica y
meníngea. Habitualmente comienza como un cuadro febril,
acompañado de escalofríos, cansancio y dolores de
cabeza. Posteriormente aparece el denominado bubón, con
hinchazón y un intenso dolor en la región corporal
afectada a la palpación de ganglios linfáticos
(sobre todo de la ingle, axila y cuello). Estas lesiones son
ovaladas, de varios centímetros de diámetro,
sobreelevadas y de color rojizo.
Lo característico del cuadro
es la brusca instalación de la fiebre y el bubón
que en el curso de pocos días puede llevar a la muerte. La
peste septicémica se caracteriza por presentar,
además de los bubones, una invasión de los
microorganismos de la circulación sanguínea con
gran repercusión del estado
general. En la de tipo neumónica se produce una de las
complicaciones más serias de la peste: la neumonía secundaria, que llega a los
pulmones a través de la sangre.
Se ha demostrado la relación de
algunas pulgas ( Xenopsylla cheopsis ) como parte
importante en el ciclo de la enfermedad. Recientemente se han
identificado 2 factores bacterianos llamados Hemin Storage
Phenotype (Hms) y Yersinia Murine Toxin (Ymt), que
juegan un importante papel en mantener el ciclo de la Y.
pestis en el vector.
Ref. ASM News, Vol.69, No.7, July
2003
Muestras Aceptables :
1. Tracto respiratorio bajo
(neumónica): Lavado bronquial o aspirado
transtraquial (= 1 ml). Las muestras de
esputo se pueden examinar pero esto no se aconseja
dado a su contaminación con flora normal de la
garganta.2. Sangre (septicémica):
Extraiga una cantidad apropiada de sangre en volumen
y número de juegos de acuerdo al
protocolo establecido del laboratorio. Nota:
en los casos en que se sospecha de plaga,
una muestra adicional de sangre o cultivo
de caldo (por lo general caldo nutriente) se debe de incubar
a temperatura ambiente (22-28 °C), la
temperatura a la cual Y. pestis crece más
rápidamente. No agite el cultivo
adicional en caldo ya que las características de la
formación de crecimientos de
Y. pestis se puedan visualizar
claramente.
Aspire una muestra de tejido
(bubónico o biopsia: hígado, bazo,
médula ósea o pulmón). Nota: los
aspirados pueden producir poco material; por lo tanto un
pequeño chorro con solución salina
estéril se puede utilizar para obtener una cantidad
adecuada de muestra. La jeringa y la aguja de la muestra
aspirada deben permanecer tapadas, aseguradas con cinta
adhesiva y enviadas al laboratorio.
Transporte de la muestra
1. Respiratoria o esputo: transporte las muestras
en contenedores estériles con tapa de
rosca a temperatura ambiente. Si se sabe que el material
será transportado de entre 2-24 horas
después de la toma de la muestra, entonces mantenga
el contenedor de transporte entre
2-8°C.
2. Sangre: Transporte las muestras directamente al
laboratorio a temperatura ambiente.
Manténgala a temperatura ambiente hasta que se coloque en
una incubadora o instrumento para cultivos de
sangre. No se refrigere. Siga los protocolos
establecidos del laboratorio para el procesamiento de cultivos
de sangre.
3. Muestras de tejido aspirado y biopsias: Remita
la muestra de tejido o aspirados en un
contenedor. Para muestras pequeñas añada de 1-2
gotas de solución salina normal para
mantener el tejido hidratado. Transporte la muestra a
temperatura ambiente para su procesamiento
inmediato. Mantenga la muestra fresca (a baja
temperatura) si se espera que su procesamiento se
retarde.
4. Hisopos: No se recomiendan las muestras de
tejidos
tomadas con hisopo. Sin embargo si se toma una
muestra con hisopo, este deberá reinsertarse en el
paquete de transporte para ser
transportado.
Frotis:
La presencia de células bipolares en
estos frotis deben de disparar la sospecha de plaga. La
tinción Wright frecuentemente revela las
características bipolares de tinción de
Y.pestis, mientras que la tinción de Gram puede
no revelarlas. La tinción Wright-Giemsa son las más
confiables para resaltar las características bipolares de
tinción de estos bacilos gram negativos.

Tinción Giemsa de frotis
sanguíneo con Y. pestis, de un paciente con
septicemia
Observe el teñido bipolar de las
células
Cultivo:
Sembrar en agar sangre de carnero, EMB,
McConkey y medio en caldo enriquecido, tal como caldo cerebro corazón (
BHI ).
Incubación de cultivos:
a. Temperatura: 28°C (óptima) ó
35-37°C (para crecimiento más lento)
b. Atmósfera:
Atmósfera ambiental, o enriquecida con COB2 Bal 5% es
aceptable
c. Duración de la incubación:
Retenga las placas primarias por cinco días. Las placas
se deben de retener hasta o por 7 días
si el paciente a recibido tratamiento con
antibióticos
bacteriostáticos.
Características:
a. Platos de agar sangre :
Y.pestis crece como colonias gris-blancas,
translúcidas, usualmente de manera pequeñas para
ser vistas como colonias individuales a 24 horas de
incubación. Después de la incubación por 48
horas, las colonias son de color gris-blanco a amarillo y opacas.
Después de 48-72 horas de incubación tienen una
apariencia elevada irregular de "huevo frito", que se vuelve
más prominente a medida que el cultivo envejece. La
hemólisis no se presenta o es muy poca en los
glóbulos rojos de cordero. Y. pestis
crecerá en colonias pequeñas no fermentadoras de
lactosa en MAC o agar EMB.
b. Tubos de caldo nutritivo : Y.
pestis crece típicamente en cúmulos que se
describen como "floculantes" o "estalactita" en apariencia cuando
el caldo de cultivo no es agitado o mezclado. Esta
característica NO es exclusiva de Y.
pestis.
Criterio de sospecha :
Cualquier muestra de cultivo aislado del
tracto respiratorio, sangre o nódulo
linfático conteniendo las
características principales que se describen más
abajo deben
considerarse sospechosas de la presencia de
Y. pestis.
1. Bacilos con características bipolares de
tinción (Wright-Giemsa) en frotis
directo.
2. Colonias del tamaño de la punta de una
aguja a las 24 horas en SBA.
3. No fermentador de lactosa, puede no ser visible
en MAC o en EMB a las 24 horas.
4. Oxidasa y ureasa negativos.
5. Catalasa positivo.
6. Frecuentemente crece mejor a
28°C.
Llave para el diagnóstico
etiológico:
Cocobacilos gram-negativos
pleomórfico.
Anaerobio facultativo.
No mótil. No
esporulado.Catalasa y Urea negativo.
TSI : K/A
No H2S. No gas.
Lactosa negativo.
Crece un poco lento.
Temperatura óptima : 28
ºC.
Limitaciones
Yersinia pestis crecerá en
un medio rico nutritivo general pero su ritmo de crecimiento es
menor que en la mayoría de otras bacterias; por
lo tanto su presencia se puede enmascarar por organismos que se
multiplican más rápidamente.
La tinción bipolar de
células no es una característica limitada a
Y. pestis; Yersinia spp, enterobacterias y otros
organismos gram negativos, principalmente Pasteurella
spp. Pueden exhibir las mismas características de
tinción.Algunos sistemas automatizados de
identificación no identifican a Y.pestis
adecuadamente. Y.pestis ha sido identificada
falsamente como Y. pseudotuberculosis, Shigella,
Salmonella HB2BS-negativa, o Acinetobacter (Wilmoth,
1996). Y. pestis produce una reacción
ácida o alcalina en medio inclinado de triple
azúcar–hierro. En la mayoría de los sistemas
comerciales convencionales de identificación el
organismo aparece como relativamente inerte haciendo que
pruebas bioquímicas posteriores sean de poco
valor.
UDiagrama de flujo para identificar Y.
pestis


Peste Bubónica

Peste Negra

Yersinia pestis
Tips:
Diagnóstico: Tinción
bipolar, apariencia de pin de seguridad en Wright´s o
Giemsa.Cultivo de sangre, esputo, o aspirado
de nodulos.Serología en estadíos
Agudo/convalesciente.Fluorescencia directa. (
Antígeno F1 )Título de > 1:128 en
suero.

Cultivo de Yersinia pestis de 72h con
apariencia de huevo estrellado
Vacuna :
No se produce desde 1990.
No disponible para uso
masivoNo sirve para forma
neumónicaNo sirve después de la
exposiciónRequiere múltiples
dosis
c) BOTULISMO:
Descripción del
organismo:
Clostridium Botulinum es un grupo
de organismos anaerobios estrictos, que se encontran
comúnmente en suelos y los
habitat acuáticos a través del mundo. Ellos son
parecidos y solo son semejantes en que pertenecen al género
clostridia y producen neurotoxinas antigenicamente distintas, con
acciones
farmacológicas similares. C. botulinum es un
organismo bacilo Grampositivo, mótil, anaerobio, con
espora oval-subterminal. Los siete tipos de C. botulinum
(A – G) se distinguen por las características antigenicas
de las neurotoxinas que producen. El botulismo humano es causado
sobre todo por cepas de C. botulinum que producen los
tipos A, B, y E de la toxina, pero los casos raros del tipo F
también se han divulgado.
En la evaluación clínica hay
que descartar el sindrome de Guillain-Barré y miastenia
gravis Los exámenes pueden incluir Scan de cerebro, examen
de LCR, electroencefalograma. La vía más directa
para confirmar el diagnóstico es la demostración de
la toxina del botulismo en suero o heces. También se puede
confirmar con animales de laboratorio ( ratones ). La bacteria
puede ser aislada en las heces de personas enfermas e infantes
con botulismo, pero requiere confirmación.
La toxina botulínica del
Clostridium botulinum es termolábil, produce una
parálisis flácida aguda, simétrica,
descendente, con efectos en 12 a 36 horas desde la
exposición. La dosis infectiva es baja de 0.001 (g/kg. Su
efecto más importante es la parálisis respiratoria.
Los pacientes requieren apoyo de ventilación mecánica por semanas o meses. La Antitoxina
no está disponible en el país.

Clostridium
botulinum
Hay tres clases principales de
botulismo:
El botulismo transmitido por los
alimentos ocurre cuando una persona ingiere la toxina
preformada que conduce a la enfermedad entre unas pocas horas
a días.El botulismo infantil ocurre cada
año en un número pequeño de lactantes
susceptibles quienes hospedan TClostridium botulinumT en su
tracto intestinal.El botulismo en la herida ocurre cuando
las heridas están infectadas por TClostridium
botulinumT que secreta la toxina.
Sintomatología :
Con el botulismo transmitido por los
alimentos, los síntomas empiezan entre 6 horas a 2 semanas
(más comúnmente entre 12 y 36 horas) después
de comer los alimentos que contienen la toxina. Los
síntomas del botulismo incluyen :
Doble visión
Visión borrosa
Párpados
caídosDificultad para hablar y dificultad
para tragarSensación de sequedad en la
bocaDebilidad muscular que siempre
desciende a través del cuerpo: primero los hombros son
afectados, luego la parte superior de los brazos, la parte
inferior de los brazos, los muslos, las pantorrillas,
etc.
La parálisis de los músculos respiratorios puede causar que una
persona pare
de respirar y muera, a menos que se proporcione asistencia para
la respiración (ventilación mecánica). El botulismo no se transmite de
una persona a otra. El botulismo transmitido por los alimentos
puede ocurrir en todas las edades.
El CDC mantienen un suministro de la
antitoxina contra el botulismo. La antitoxina es eficaz en
reducir la gravedad de los síntomas si se administra a
principios del
curso de la enfermedad. La mayoría de los pacientes se
recuperan después de semanas a meses de atención médica adecuada.
Muestra
Tipos de muestras aceptables
1. Muestras clínicas
2. Muestras post mortem
3. Cultivos o aislamientos
4. Muestras de alimentos sólidos o
líquidos
5. Muestras ambientales
Procedimiento :
1. Heces: Coloque una cantidad de
heces del tamaño de una nuez en un contenedor
irrompible y etiquételo cuidadosamente. La evidencia
confirmatoria de botulismo se puede obtener de
muestras de heces de 10 a 50 g.
2. Enema: Coloque aproximadamente 20
ml de líquido extraído por enema en un
contenedor estéril, irrompible y etiquételo
cuidadosamente. Se debe evitar que el material con la toxina se
diluya innecesariamente.
3. Vómitos y
aspirados gástricos : Coloque 20 ml en un contenedor
estéril e irrompible y etiquételo
cuidadosamente.
4. Suero: Use tubos sin
anticoagulante para obtener suero. Las muestras se deben de
obtener tan pronto como se presenten los síntomas pero
antes de administrada la antitoxina. Se debe centrifugar la
sangre y colectar el suero, el que será enviado a un
laboratorio especializado.
5. Tejidos o exudados:
Colóquese dentro de un contenedor irrompible y
estéril y etiquételo cuidadosamente.
La muestra se deberá colocar en un frasco
Port-A-Cult y envíese al laboratorio
apropiado, preferentemente sin refrigeración para intentar el aislamiento
de C. botulinum.
6. Post mortem: Obtenga muestras
intestinales de diferentes niveles de ambos
intestinos. Coloque 10 g. por muestra en un frasco
estéril e irrompible etiquetado
cuidadosamente. Obtenga ya sea contenido
gástrico, suero, tejido o muestras de tejidos
siempre y cuando sea apropiado.
7. Cultivo: Envíe cultivos
aislados sospechosos anaeróbicamente (cubra el
medio líquido con una capa de 2 pulgadas de
parafina fundida. Los cultivos se pueden enviar a temperatura
ambiente o refrigerados.
8. Muestras de alimentos: Los
alimentos se deben de dejar en su contenedor original
de ser posible o colocarse en contenedores estériles
e irrompibles etiquetados cuidadosamente. Coloque
los contenedores individualmente a prueba de fugas
(por ejemplo: bolsas plásticas selladas) para
prevenir la contaminación cruzada durante su
transportación.
9. Muestras con hisopos (ambientales o
clínicos): Envíe los hisopos clínicos en
un medio de transporte anaeróbico (por
ejemplo: Tubos Port-A-Cult). Los hisopos ambientales (de los
cuales se pueden aislar esporas) se pueden enviar en contenedores
plásticos
sin medio alguno. Los hisopos se pueden enviar a temperatura
ambiente o refrigerados. Tome muestras con 3 a 4 hisopos de cada
lugar potencial.
10. Muestras ambientales: Tome el
tamaño de muestra que se indica para cada posible
ubicación
(1) Suelo (50-100
g)
(2) Agua (= 100 ml)
11. Liberación intencional de
toxina (por inhalación o ingerida) :
a. Suero
b. Heces obtenidas mediante enema con agua
estéril
c. Alimento sólido o
líquido
d. Hisopo nasal o muestra
ambiental
e. Aspirado de contenido
gástrico
Información relacionada con la
muestra :
1. Alimentos
Los alimentos en los que se espera que se
desarrolle con mayor probabilidad C.
botulinum, son aquellos que tienen un rango general de
pH
de 3.5 a 7.0, siendo un rango de pH más común
el de 5.5 a 6.5. Sin embargo los alimentos en los
que se sospecha la presencia de C. botulinum,
independientemente de su pH podrían ser examinados,
dado que condiciones ambientales localizadas que
pudieron estar presentes en el alimento,
podrían sostener el desarrollo de C.
botulinum.
La toxina botulínica en productos
comerciales es rara. El laboratorio deberá notificar a las
autoridades si se sospecha que un producto comercial se encuentra
contaminado con la toxina botulínica.
2. Heces: C. botulinum ha sido
aislado de muestras de heces fecales obtenidas
seguidamente del tratamiento con antitoxinas. Acto seguido,
enviar la muestra a
un laboratorio capaz de detectar la toxina
del C. botulinum, utilizando el protocolo de
envío de muestras peligrosas.
NOTA : En caso de contacto con el CDC de
Atlanta : National Botulism Surveillance and Reference
Laboratory: Tel. ( 001 )-404-639-3867.
 Página anterior Página anterior |   Volver al principio del trabajo Volver al principio del trabajo | Página siguiente  |
